

【研究背景】
隨著工業(yè)化的發(fā)展,環(huán)境污染物對(duì)人類健康的威脅日益顯著。內(nèi)分泌干擾化合物(EDCs)是一類廣泛存在于土壤和水系統(tǒng)中的新型環(huán)境污染物,對(duì)人類的生殖和內(nèi)分泌系統(tǒng)造成嚴(yán)重影響。在中國(guó),EDCs在地表水環(huán)境中的濃度遠(yuǎn)超歐盟標(biāo)準(zhǔn),對(duì)水質(zhì)和人體健康構(gòu)成嚴(yán)重威脅。慢性腎臟病(CKD)是一種全球性公共衛(wèi)生問(wèn)題,其發(fā)病率高且預(yù)后差。研究表明,EDCs與CKD的發(fā)生發(fā)展密切相關(guān),但具體的潛在靶標(biāo)和毒理學(xué)機(jī)制尚不清楚。本研究旨在利用網(wǎng)絡(luò)毒理學(xué)和分子對(duì)接技術(shù),探討常見(jiàn)的EDCs(壬基酚NP和辛基酚OP)在CKD發(fā)生中的潛在毒性靶標(biāo)和分子機(jī)制。
【研究方法】
研究結(jié)合網(wǎng)絡(luò)毒理學(xué)和分子對(duì)接技術(shù),利用CTD和GeneCards數(shù)據(jù)庫(kù)獲取NP和OP的潛在靶標(biāo),并進(jìn)行基因集富集分析。通過(guò)STRING數(shù)據(jù)庫(kù)和Cytoscape軟件構(gòu)建蛋白質(zhì)相互作用網(wǎng)絡(luò),識(shí)別核心靶標(biāo)。進(jìn)一步利用GEO數(shù)據(jù)庫(kù)中的CKD數(shù)據(jù)集GSE66494,構(gòu)建基于核心靶標(biāo)的診斷模型,并進(jìn)行校準(zhǔn)和ROC曲線分析以評(píng)估模型的診斷價(jià)值。通過(guò)分子對(duì)接和分子動(dòng)力學(xué)模擬驗(yàn)證核心靶標(biāo)與NP和OP的結(jié)合穩(wěn)定性。
【研究結(jié)果】
u NP和OP的基因富集分析:
研究發(fā)現(xiàn)NP和OP的靶標(biāo)基因主要與氧化應(yīng)激、炎癥反應(yīng)和免疫調(diào)節(jié)等生物功能密切相關(guān)。KEGG富集分析顯示,這些靶標(biāo)基因在TNF信號(hào)通路、MAPK信號(hào)通路和IL-17信號(hào)通路中顯著富集。

u 核心靶標(biāo)識(shí)別:
通過(guò)與CKD相關(guān)的靶標(biāo)基因?qū)Ρ龋l(fā)現(xiàn)49個(gè)核心靶標(biāo)基因,這些基因與氧化應(yīng)激、炎癥和凋亡等生物過(guò)程密切相關(guān)。

u 蛋白質(zhì)相互作用網(wǎng)絡(luò)和關(guān)鍵基因識(shí)別:
利用Cytoscape軟件,研究識(shí)別出五個(gè)關(guān)鍵基因:TNF、MAPK3、ESR1、FOS和BCL2。

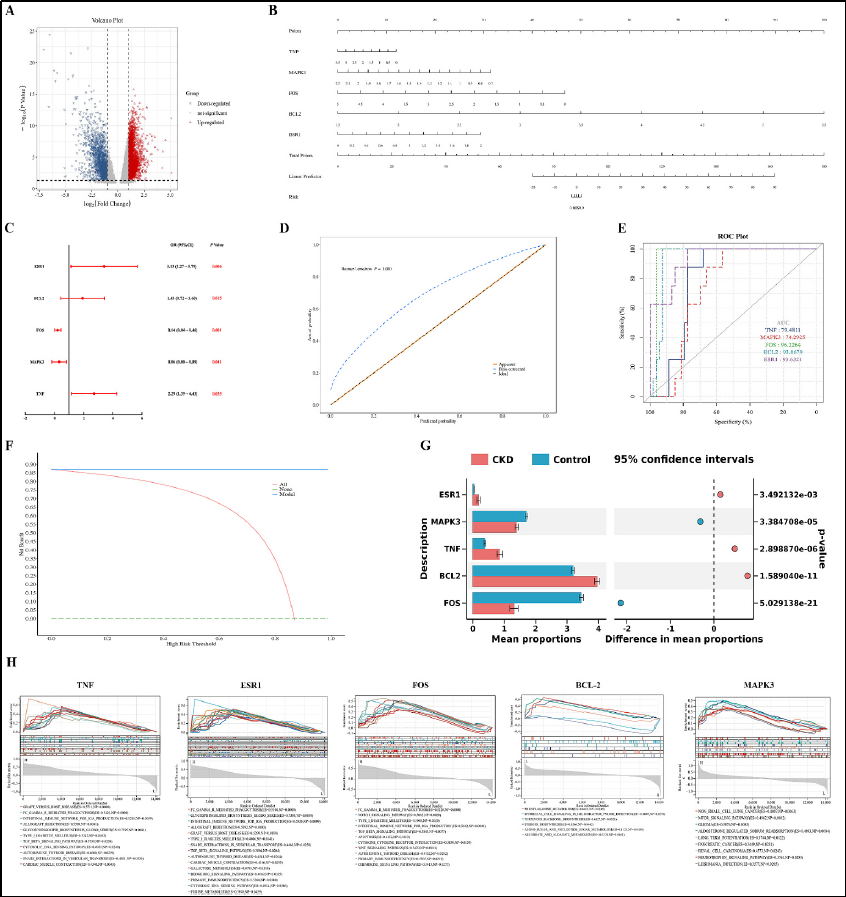
u 關(guān)鍵基因的診斷模型構(gòu)建:
基于這五個(gè)關(guān)鍵基因構(gòu)建的列線圖模型在CKD診斷中表現(xiàn)良好,校準(zhǔn)曲線和ROC曲線均顯示模型具有良好的診斷價(jià)值。
u 單基因GSEA富集分析:
五個(gè)關(guān)鍵基因通過(guò)影響多種生物途徑參與CKD的發(fā)展,其中多個(gè)免疫相關(guān)信號(hào)通路顯著富集。
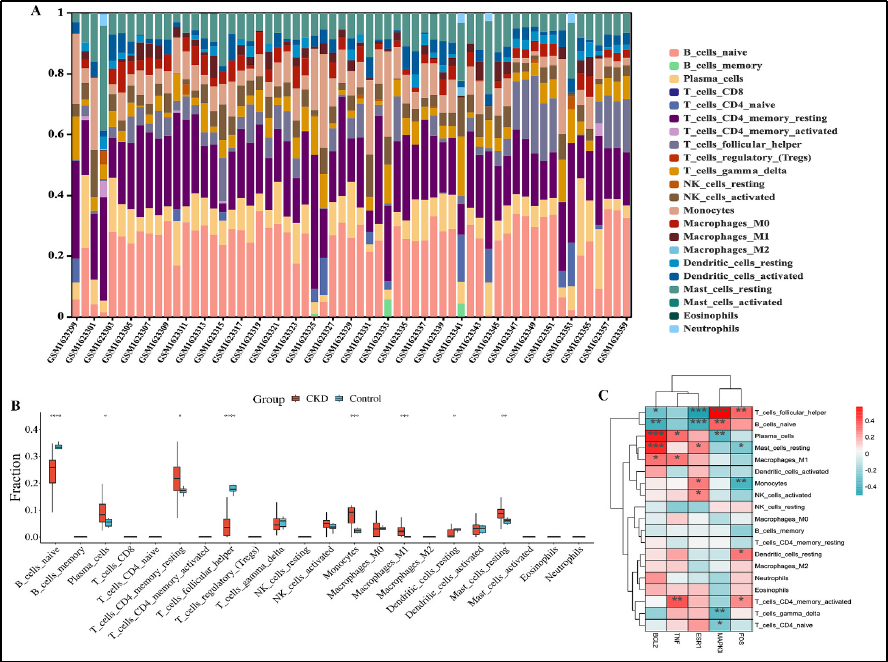
u 免疫細(xì)胞浸潤(rùn)分析:
研究發(fā)現(xiàn)八種免疫細(xì)胞在CKD中的浸潤(rùn)水平顯著變化,關(guān)鍵基因與多種免疫細(xì)胞的浸潤(rùn)水平密切相關(guān)。
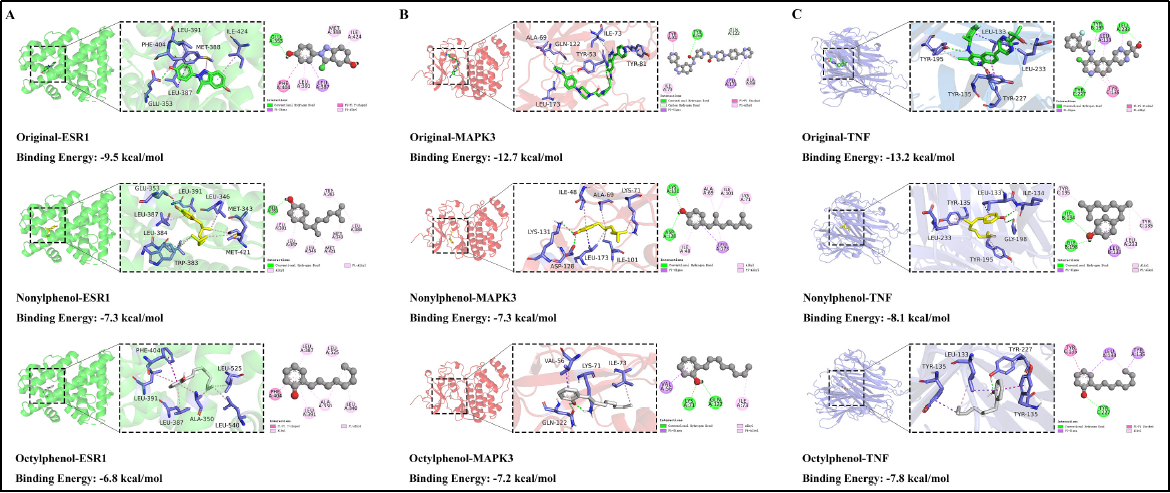
u 分子對(duì)接結(jié)果:
分子對(duì)接結(jié)果表明,ESR1(-6.8 kcal/mol)、MAPK3(-7.2 kcal/mol)和TNF(-7.8 kcal/mol)與NP和OP的結(jié)合能zui低,表明這些蛋白是NP和OP的主要作用靶標(biāo)。
u 分子動(dòng)力學(xué)模擬分析:
分子動(dòng)力學(xué)模擬進(jìn)一步驗(yàn)證了ESR1、MAPK3和TNF蛋白與NP和OP之間相互作用的穩(wěn)定性。
均方根偏差(RMSD)分析:RMSD曲線顯示,NP、OP與ESR1蛋白形成的復(fù)合物的RMSD值在整個(gè)模擬過(guò)程中保持在約0.2nm范圍內(nèi),表明該復(fù)合物結(jié)構(gòu)穩(wěn)定。在MAPK3組中,NP與MAPK3蛋白的RMSD曲線波動(dòng)最小,穩(wěn)定性優(yōu)于共晶配體。OP與MAPK3蛋白的RMSD曲線在45ns處有小幅波動(dòng)后恢復(fù)穩(wěn)定,波動(dòng)范圍約0.3nm。TNF組中,NP和共晶配體與TNF蛋白的RMSD曲線幾乎wan全重疊,穩(wěn)定性接近且較強(qiáng),OP與TNF蛋白的RMSD曲線波動(dòng)范圍略大,但仍小于0.3nm,表明OP與TNF的結(jié)合穩(wěn)定性略低于NP和共晶配體。
均方根波動(dòng)(RMSF)分析:RMSF曲線顯示,所有復(fù)合物中氨基酸殘基的波動(dòng)程度均小于1nm,表明復(fù)合物整體穩(wěn)定性良好。
回轉(zhuǎn)半徑(Rg)分析:Rg曲線顯示,所有復(fù)合物的Rg值在模擬過(guò)程中波動(dòng)較小,分別穩(wěn)定在約1.85nm、2.05nm和2.15nm,表明復(fù)合物結(jié)構(gòu)緊密且穩(wěn)定。
氫鍵數(shù)量分析:在ESR1組中,NP、OP與ESR1蛋白形成的復(fù)合物的氫鍵數(shù)量分別穩(wěn)定在約1-2、1和2個(gè)。在MAPK3組中,NP、OP與MAPK3蛋白形成的復(fù)合物的氫鍵數(shù)量均穩(wěn)定在約1-2個(gè)。在TNF組中,共晶配體與TNF蛋白形成的復(fù)合物的氫鍵數(shù)量穩(wěn)定在約2-3個(gè),而NP、OP與TNF蛋白形成的復(fù)合物的氫鍵數(shù)量均穩(wěn)定在約1-2個(gè)。這表明所有復(fù)合物均形成了良好的氫鍵網(wǎng)絡(luò),增強(qiáng)了結(jié)合的穩(wěn)定性。
自由能分布分析:自由能分布圖顯示,NP和OP與ESR1、MAPK3和TNF蛋白形成的復(fù)合物均形成了單一且平滑的zui低能量簇,表明這些復(fù)合物具有較高的結(jié)合穩(wěn)定性。其中,OP與TNF蛋白形成的復(fù)合物的自由能分布圖出現(xiàn)了多個(gè)zui低能量簇,表明其結(jié)合穩(wěn)定性略低于其他復(fù)合物。
結(jié)合自由能計(jì)算:使用MM/GBSA方法計(jì)算的平均結(jié)合自由能顯示,ESR1與NP、OP的結(jié)合自由能分別為-30.27 kcal/mol和-26.33 kcal/mol;MAPK3與NP、OP的結(jié)合自由能分別為-36.78 kcal/mol和-35.82 kcal/mol;TNF與NP、OP的結(jié)合自由能分別為-44.51 kcal/mol和-43.67 kcal/mol。這些負(fù)值表明NP和OP與蛋白結(jié)合緊密,其中NP與MAPK3蛋白的結(jié)合自由能zui低,表明MAPK3可能是NP的最佳結(jié)合靶標(biāo)。
綜上所述,分子動(dòng)力學(xué)模擬結(jié)果證實(shí)了NP和OP與ESR1、MAPK3和TNF蛋白之間相互作用的穩(wěn)定性,其中NP與MAPK3蛋白的結(jié)合尤為穩(wěn)定。這些發(fā)現(xiàn)為理解NP和OP在CKD中的潛在毒性機(jī)制提供了重要的結(jié)構(gòu)基礎(chǔ)

【研究結(jié)論】
本研究通過(guò)網(wǎng)絡(luò)毒理學(xué)和分子對(duì)接技術(shù),識(shí)別出NP和OP在CKD中的五個(gè)關(guān)鍵基因TNF、MAPK3、ESR1、FOS和BCL2,并構(gòu)建了具有良好診斷價(jià)值的列線圖模型。分子對(duì)接和分子動(dòng)力學(xué)模擬結(jié)果表明,NP和OP與這些關(guān)鍵基因具有良好的結(jié)合親和力和穩(wěn)定性,暗示它們可能是NP和OP誘導(dǎo)CKD的主要作用靶標(biāo)。這些發(fā)現(xiàn)不僅為理解NP和OP在CKD中的潛在毒性機(jī)制提供了理論依據(jù),還推動(dòng)了網(wǎng)絡(luò)毒理學(xué)和分子對(duì)接技術(shù)在環(huán)境污染物研究中的應(yīng)用。
然而,研究也存在局限性,如未涵蓋所有EDCs且結(jié)果需臨床研究進(jìn)一步驗(yàn)證。
Pei J, Peng J, Wu M, Zhan X, Wang D, Zhu G, Wang W, An N, Pan X. Analyzing the potential targets and mechanisms of chronic kidney disease induced by common synthetic Endocrine Disrupting Compounds (EDCs) in Chinese surface water environment using network toxicology and molecular docking techniques. Sci Total Environ. 2025 Jan 1;958:177980. doi: 10.1016/j.scitotenv.2024.177980. Epub 2024 Dec 9. PMID: 39657341.
歡迎您關(guān)注我們的微信公眾號(hào)了解更多信息
 掃一掃
掃一掃